猪病百科:猪流行性腹泻防控16法则
porcine epidemicdiarrhea virus, PEDV)引起的猪的一种急性、高度接触性、传染性的肠道疾病,该病以严重的肠炎、呕吐、水样腹泻和脱水为主要特征,各种日龄的猪均易感,尤其是哺育仔猪,发病率高达毒株其毒力和致病性等出现异化,如夏天也在一些地方零星爆发从临床样本中也分离到了毒力与致病性迥异的),这极度影响了我国养猪业的健康发展。因此,对该病及其病原的研究具备极其重大的意义。
猪流行性腹泻病(PEDV)属于尼多病毒目(Nidovirales)、冠状病毒科(Coronaviridae)、冠状病毒属a群成员。2008年,将冠状病毒分为三个抗原群,即α群、β群、γ群。
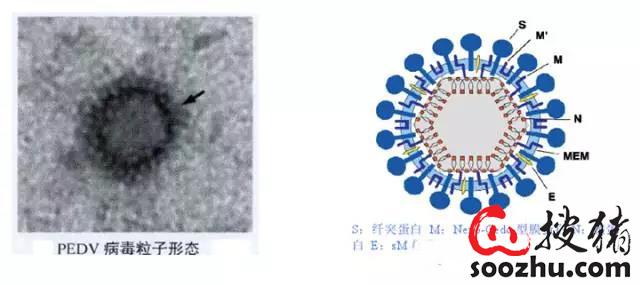
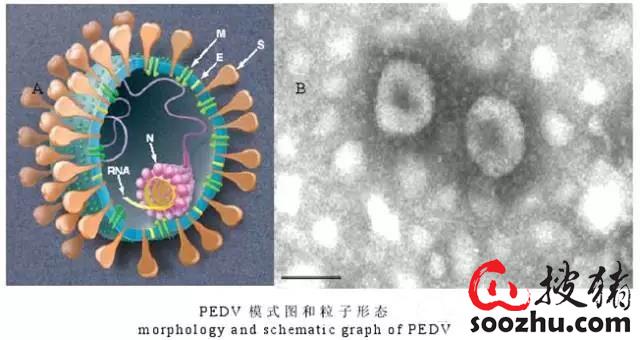
PEDV病毒粒子的形状呈现多形性,病料分离的多为球星,直径大小为95---190nm(包括纤突);PEDV是有囊膜的、不分节段的、单股正链RNA病毒,其基因组大小约为28 nt。具有4种结构蛋白:纤突蛋内(S)、膜蛋内(M)、小包膜蛋内(E)、核衣売蛋白(N)。
可以在胎猪肠组织原代单细胞、肾脏原代细胞、ESK、CPK和MA104的传代细胞系中进行增值,并产生非常明显的CPE。
PEDV的抵抗力不强,一般消毒剂即可将其致死,如甲酚、2%的氧氧化钠、、过氧乙酸(瑞福星);对脂溶性溶剂(如和氯仿)敏感,不凝集猪、犬、马、绵羊、山羊、母羊、兔、鼠、雏鸡、和人等的红细胞。在pH值为5--9、温度为4°C时或者当pH值为6.5--7.5、温度为37°C时,PEDV粒都可以稳定存在。
目前,所有已分离到的PEDV毒株都属于同一个血清型,但并不能排除PEDV还有别的血清型的可能性。
PEDV基因组RNA的点突变、插入、缺失和不同毒株之间的同源重组是PEDV变异的主要分子基础。目前的研究表明:PEDV的S基因、N基因、0RF3基因在病毒的进化上均表现出变异现象。S基因的变异最明显,S基因不仅存在点突变、还存在插入、缺失和重组现象,N基闪只存在点突变和不同毒株之间的同源重组,而0RF3基因除了存在点突变之外,还有缺失现象。
目前,抗PEDV的免疫机制仍不清楚,预防PED大范围的应用的免疫方法主要是对怀孕母猪进行免疫接种,通过母源抗体让仔猪获得人工被动免疫保护。由于PEDV有肠道组织嗜性,所以,在抗PEDV感染免疫过程中,除细胞免疫和体液免疫外,肠粘膜免疫系统也发挥着无法替代的作用。我国研制的PED和TGE系列疫苗均采用了猪后海穴免疫接种,这种免疫接种途径除激活细胞免疫和体液免疫外,同时也激活了肠道局部粘膜免疫,所以与常规免疫接种途径相比免疫效果更佳。
PEDV复制场所大多分布在在猪小肠绒毛上皮细胞中,其利用表面的S蛋白与猪小肠绒毛上皮细胞上的表面受体结合,并利用膜融合入侵到细胞内,并在细胞浆中大量复制。感染猪通过粪便和呕吐物将新生的病毒排出体外。研究证实,猪可溶性APN在体外能提高PEDV在Vero细胞中病毒含量,说明在增强PEDV的感染性和增殖能力方面猪氨基肽酶N(pAPN)具备极其重大的作用。
自2011年3月至今,猪病毒性腹泻在我国大范围爆发,中国农业科学院哈尔滨兽医研究所猪病毒性腹泻课题组利用胶体金试纸条,RT-PCR,强、弱毒鉴别等诊断方法结合基因序列测定分析了国内11个省、市猪场腹泻病例,检测结果为,PED阳性率占54.7 %、TGE的阳性率为38.1 %,两者的混合感染率为25.9 %,猪轮状病毒(PoRV)的阳性率为5.04 %,而猪嵴病毒(Kobuvirus)的阳性率只有1.44 %,综合仔猪的临床发病症状(呕吐、腹泻和脱水)以及病料的检测根据结果得出PED在我国猪病毒性腹泻感染中占主导地位(陈建飞等,2011)。
传播途径多样化:PEDV主要是通过运输病猪或者带毒猪或者被其污染的词料、车辆及其被病毐污染的鞋和其他携带病毐的污染物、感染猪的粪便传入猪群;
主要传染源是病猪和带毒猪,病源通过病猪或者带毒猪排泄的粪便经鼻-口途径感染健康猪。
易感动物所有的猪均可受到感染,哺乳乳猪发病率和病死率通常为100%。主要侵害7日龄以内仔猪。仔猪出生后2~3天(最短是出生后6小时)发病,表现为水样腹泻、脱水和部分仔猪呕吐;
猪是PEDV唯一的自然宿主。此病主要发生于冬末春初的寒冷季节,但是夏季高温时节也有发生和流行。。
发病范围广(全国所有养猪省份);时间跨度大、发病维持的时间长,一年四季均发生;反复发作,间隔2-3周又有新的哺乳仔猪群发病;
强毒免疫(返饲)效果不好;(由于我国温和型猪瘟、野毒的伪狂犬、蓝耳和圆环带毒,建议建议还是不要采纳)。
该病的病原毒力显著地增强。临床发现,如果猪场有该病流行,即使母猪的抗体水平很高,也不能对乳猪进行相对有效保护。推测可能是潜伏期缩短,猪流行性腹泻病毒(PEDV)提前初乳到达肠道。临床实验表明,如果乳猪超前(出生后马上灌服抗体+头孢)灌服抗体,则效果明显。
该病的典型症状是水样腹泻,在部分国家或地区的种猪场中,如果该病经常流行或母猪群免疫良好,则新出生的仔猪罕见暴发PED。实验感染猪的潜伏期为8~24 h,自然感染则稍长些。病猪首先表现呕吐,多发生在哺乳或吃食后,吐出的胃内容物呈黄色或乳白色。随后出现水样腹泻,腹泻物呈灰黄色、灰色,或呈透明水样,顺肛门流出,并玷污臀部。病猪表现脱水、眼窝下陷、行走蹒跚、精神沉郁、食欲减退或停食。症状与年龄大小有关,年龄越小症状越严重。新生仔猪感染后常发生严重失水和死亡,平均病死率为50 %,但有时高达100 %。断乳猪、育肥猪以及母猪症状较哺乳仔猪轻,表现精神不振、厌食、持续腹泻4~7d后逐渐回到正常状态,少数猪生长发育不良。
剖检主要病变为小肠高度膨胀,内部充满淡黄色液体,肠壁变薄,有时个别小肠黏膜有出血点,肠系膜淋巴结水肿,小肠绒毛变短,严重者绒毛萎缩,甚至消失。胃内经常是空的,或充满胆汁样的黄色液体。其他实质性器官无明显病变。
到目前为止,氨基肽酶(aminopeptidaseN,APN)已被证明为多种冠状病毒的受体,如TGEV、PEDV、HCOV-229E、FeCoV等都以氨基肽酶(APN)作为其细胞感染受体,APN与病毒的纤突蛋白结合,并使病毒进入细胞。因此在致病特性上,冠状病毒有着非常明显的呼吸道和消化道等特异的组织嗜性,从而引起临床的呼吸道疾病和消化道腹浑性疾病。幼龄动物之所以对冠状病毒感染更为敏感,是因为其粘膜表面的受体物质比成年动物更丰富。不同种属的APN的活性范围往往仅有一个或儿个氨基酸所决定,一个或几个氨基酸的改变即可对整个受体的结构和活性造成影响,因此改变受体上氨基酸的数量或突变氨基酸都会改变受体的活性或宿主范围。
PEDV可通过消化道进入机体,经血清学和分子生物学检测,表明PEDV利用氨基肽酶(aminopeptidaseN,APN)在小肠和结肠的绒毛上皮细胞浆中进行增殖。在复制过程中首先使细胞器受损,继之使细胞功能发生障碍,产能减少,进而加重上皮细胞的损伤。还可导致肠绒毛萎缩、变短,致吸收表面积减少,引起吸收营养的东西的机能显著障碍,从而导致腹泻的发生,引起脱水,使病猪衰竭死亡。现在还不清楚,结肠感染在多大程度上可以加剧临床症状和发生在出栏猪和成年猪伴有的急性背肌坏死而导致突然死亡的发病机制。
本病仅依据临床、病理变化和流行病学很难做出诊断,特别是与TGE不易区别,必须依靠实验室技术才能做出准确的判断。
可对腹泻仔猪粪便样品进行直接电镜观察,但若病毒的纤突丧失或不清晰,直接电镜检查较为困难。在人工感染的仔猪中,于腹泻发生后第一天收集的粪便中PEDV的阳性检出率最高,为73 %。由于PEDV和TGEV的形态相同,已建立了免疫电镜用于区别这两种病毒。
在现地可用ELISA方法对成年猪和仔猪的粪便和肠内容物进行仔细的检测,结果敏感可靠。此法最好在腹泻的急性期收集几个不同猪的粪便作检查。检测血清抗体做回归性诊断有两种方法:猪小肠PEDV阳性冷冻切片的间接免疫荧光试验和酶联免疫吸附试验。这两种检测的新方法都应该检测双份血清,第二份血清必须采自发生腹泻4周后的康复后血清。PED的抗体可在血清中保持1年以上,但是在第一次感染后5个月的血清阳性猪群中能引起伴有腹泻的再感染。
欧洲在PED爆发期间,有意的让怀孕母猪接触感染后死亡小猪的肠内容物,人为地刺激母猪产生乳汁免疫,以希望缩短PED爆发在猪场的维持的时间(Pensaert and Yeo, 2006)。然而,这种治疗方法有以下缺点:
(3)可以通过污染其他病毒性病原(猪繁殖和呼吸道综合症病毒和猪圆环病毒2型等)而引起其他疾病传播。(2013年3月惠州某规模化猪场因此使整个猪场感染猪瘟。)
接种疫苗是目前预防本病有效而可靠地办法之一。猪场爆发PED时,主要防治措施有:
(1)疫苗:在此病流行地区的流行季节之前,全群进行免疫,最好是母猪分娩前连续两次的肌肉注射免疫,乳猪后海穴免疫。
(2)管理:加强饲养管理,改善猪舍环境(温度、湿度、光照等),保持猪舍温暖清洁和干燥,猪舍空气清新,猪场常消毒,确保饲料质量,不可以使用霉变的饲料。
(3)治疗:本病流行速度很快,病猪食欲废绝,应及时补充含有葡萄糖、氯化钠、碳酸氢钠等饮水,阿托品等辅助治疗,并确保饮水的清洁,减轻脱水的压力。如果管理条件得到一定效果改善,通常可以在一周内控制疫情,否则,病程拖长,而且增加了死亡率。
本病最佳的治疗时机:治疗时必须在未出现症状前(建议根据猪场发病日龄,提前1-2天,一定要在肠粘膜未损伤前效果明显)注射新城疫1系(50羽,7日龄乳猪)+左旋咪唑0.75mg/kg,或者黄芪多糖注射液(注射后10小时左右产生很好的干扰素,维持的时间长);同时灌服(300g淡附子+200g干姜+300g甘草等煎服,注意附子的毒性处理,400头7日龄乳猪一次的口服量,1次/日,连续3-5天)。目前有效率70-90%。